Μετάφραση Αργυρώ Βεργανελάκη
|
|
Ένας από τους πολλούς ρόλους των φυσικών επιστημών είναι να υποστηρίζουν τις θεωρητικές σπουδές. Έχοντας αυτό κατά νου, ο Gianluca Farusi και οι μαθητές του αποφάσισαν να ερευνήσουν και να παρασκευάσουν μελάνι από όζο σιδήρου, ένα πολύ σημαντικό ιστορικά υλικό για την μετάδοση της γνώσης. |
Ιστορική αναδρομή
Πολλές μεσαιωνικές μινιατούρες του Αγ. Ιωάννη στην Πάτμο, δείχνουν την σημασία του μελάνιού : αναπαριστούν το Διάβολο να προσπαθεί να κλέψει το πολύτιμο μελάνι του αγίου. Κατά το μεσαίωνα δύο είδη μελανιού χρησιμοποιούνταν : μελάνι άνθρακα (ένα μίγμα άνθρακα, νερού και κόμμιου) και μελάνι από όζο σιδήρου (προερχόμενο από όζους βελανιδιάς). Το μελάνι άνθρακα εμφανίστηκε γύρω στο 2500 π.Χ. ενώ το μελάνι από όζο σιδήρου χρησιμοποιήθηκε από τον 3ο αιώνα μ.Χ. και μετά, από προσωπικότητες όπως οι Leonardo da Vinci, Johann Sebastian Bach, Rembrandt van Rijn και Vincent van Gogh. Σύμφωνα με πρόσφατη έρευνα, ίχνη μελάνης από όζο σιδήρου έχουν βρεθεί σε πάπυρους της Νεκράς θάλασσας και στο χαμένο Ευαγγέλιο του Ιούδαw1.
Η αντίδραση που δίνει την χρωστική του μελανιού δεν χρησιμοποιούταν στον αρχαίο κόσμο για την παραγωγή μελανιού, αλλά ήταν ήδη γνωστή: στην NaturalisHistoria(Φυσική Ιστορία) του ο Pliny ο Γηραιότερος (23-79 μ.Χ.) περιγράφει πώς να ξεχωρίζουμε την πρασινάδα χαλκού [Cu(CH3COO)2.2Cu(OH)2], που χρησιμοποιείται στην κατεργασία δέρματος, από την φθηνότερη καραμπογιά (FeSO4.7H2O) με την οποία νοθευόταν συχνά. Γράφει:
“…Η απάτη μπορεί να αποκαλυφθεί χρησιμοποιώντας ένα φύλλο πάπυρου βουτηγμένο σε υγρό από όζο καρυδιάς: γίνεται κατευθείαν μαύρο όταν εφαρμόζεται η νοθευμένη πρασινάδα χαλκού”.
Παρά το γεγονός ότι έβλεπε την αλλαγή, δεν μπορούσε να την κατανοήσει. Τώρα γνωρίζουμε ότι αυτό το αρχαίο τεστ στηρίζεται στην αντίδραση ανάμεσα στο κατιόν σιδήρου (σίδηρος( ΙΙ )) και στο γαλλοτανικό οξύ που υπάρχει στη ρίζα του παρασκευάσματος μελανιού από όζο σιδήρου (δείτε παρακάτω).
Το εκπαιδευτικό περιεχόμενο
Όταν ένας από τους μαθητές μου στη χημεία με ρώτησε τι είδος μελανιού χρησιμοποιούσαν οι καλόγεροι στο μεσαίωνα, εμπνεύστηκα να οργανώσω μία εργασία για το μελάνι των μοναχών (δείτε το ένθεμα). Ταυτόχρονα με την προσφορά μιας διδακτικής εκδοχής στην επιστήμη, δίνει έμφαση στους δεσμούς ανάμεσα στις φυσικές επιστήμες και τις θεωρητικές σπουδές.
Αποφασίσαμε να χρησιμοποιήσουμε τη συνταγή του Βενετσιάνου Pietro Canepario από το βιβλίο του Deatramentiscuiuscumquegeneris (Όλα τα είδη του μελανιού, 1619). Σε ιδιωματικά Ιταλικά με ομοιοκαταληξία, περιγράφει τη σύσταση κατά βάρος του μελανιού : “Una, due, tre e trenta a far la bona tenta” (“με ένα, δύο, τρία και τριάντα μέρη προσπάθησε να το κάνεις σωστά”). Τώρα γνωρίζουμε ότι αυτή η αναλογία από αραβικό κόμμι, θειικό σίδηρο, όζους και νερό δεν είναι η καλύτερη για το μελάνι από όζο σιδήρου: επειδή είναι πολύ όξινο, πολλές φορές καταστρέφει το χαρτί. Ο στόχος μου, όμως, δεν ήταν να παρασκευάσουμε το καλύτερο μελάνι, αλλά μάλλον να ενθαρρύνω τους μαθητές να ερευνήσουν την ιστορία, χρησιμοποιώντας τη χημεία και να κατανοήσουν τον πολιτιστικό και εκπαιδευτικό της ρόλο.
Στη συνέχεια οι μαθητές ερεύνησαν όζους και ξεκίνησαν να συλλέγουν κοινούς τύπους- όζους τύπου βελανιδιάς (βελανιδιάς και κουμαριάς) και όζους κυπαρισσιού – για να μας δώσουν την ευκαιρία να συγκρίνουμε τρία διαφορετικά μελάνια.
Θέλαμε να εξακριβώσουμε τον καλύτερο τύπο μελανιού, αλλά με βάση ποια κριτήρια; Αποφασίσαμε να μην απομακρυνθούμε πολύ από την εποχή του Canepario, και αναφερθήκαμε στο De subtilitate (Οι εσωτερικοί δεσμοί ανάμεσα στα πράγματα) και στο De rerum varietate (Οι ποικιλία των πραγμάτων) από τον Gerolamo Cardano (1501-1576). Σύμφωνα με τον Cardano, ένα καλό μελάνι ρέει καλά, και είναι παχύ, μαύρο και φωτεινό. Δοκιμάσαμε τα μελάνια μας, γράφοντας και με πιππέτες Pasteur και με μύτες στυλό και βρήκαμε ότι το μελάνι από όζους βελανιδιάς τηρούσε καλύτερα τα κριτήρια. Το αγαπημένο μου , όμως, ήταν αυτό του κυπαρισσιού: παρόλο που δεν είναι τόσο μαύρο όσο αυτό της βελανιδιάς, μοσχοβολάει ρετσίνι.
Βέβαια, καταλήξαμε με συζήτηση πάνω στη χημεία: αναρωτηθήκαμε ποιες αντιδράσεις παίρνουν μέρος σε κάθε στάδιο της παραγωγής, για τις επακόλουθες αντιδράσεις ανάμεσα στο μελάνι και το χαρτί, καθώς και τη σημασία τους για τα ιστορικά κείμενα και πώς θα μπορούσε να αποφευχθεί η περαιτέρω καταστροφή τους.
Οι μαθητές λάτρεψαν την εργασία, ιδιαίτερα τη διαθεματική και ιστορική εκδοχή της. Ένας μαθητής δήλωσε ότι η χημεία “ μοιάζει να είναι το κλειδί στα σύγχρονα και τα αρχαία ερωτήματα”.
Συστατικά του μελανιού από όζο σιδήρου
|
|
|
|
|
Εικόνα 1: Όζος βελανιδιών |
Εικόνα 2: Όζος κουμαριάς |
Εικόνα 3: Όζος κυπαρισσιού |
Η πρώτη συγκεκριμένη αναφορά στο μελάνι από όζο σιδήρου γίνεται στο βιβλίο του Martianus Minneus Felix Capella “De Nuptiis Philologiae et Mercurii et de septemArtibus liberalibus libri novem”, 420 μ.Χ.), που αναφέρεται σε ένα μίγμα από όζο και κόμμι. Παρόλο που και άλλες συνταγές διατηρήθηκαν, όλες συμφωνούν στα βασικά συστατικά: όζοι, θειικός σίδηρος (καραμπογιά), νερό και αραβικό κόμμι.
Όζοι
Οι όζοι είναι ανώμαλα εξογκώματα που υπάρχουν πάνω στα φύλλα, στους μίσχους, στα λουλούδια και στις ρίζες φυτών. Ο παράγοντας που προκαλεί το σχηματισμό τους, συνήθως μία μύγα ή σφίγγα, εναποθέτει ένα αυγό στον νεαρό φυτικό ιστό, και ο όζος σχηματίζεται γύρω από τη λάρβα, που τρέφεται κα αναπτύσσεται μέσα στον προστατευτικό σχηματισμό. Οι εκκρίσεις από τη λάρβα, συμπεριλαμβανομένων σάλιου και αποβλήτων, πιστεύεται ότι ελέγχουν την ανάπτυξη του σχηματισμού.
Η χημική σύσταση του όζου ποικίλει ανάλογα με τον παράγοντα που τον σχηματίζει και το συμμετέχον φυτό. Ο όζος από τη λεπτομονάδα Aleppo είναι πλούσιος σε ταννικό οξύ (65%) και γαλλικό οξύ (2%) ˙ ο όζος της Βασόρας (γνωστό και ως γεώμηλο) περιέχει 26% ταννικό οξύ και 1,6% γαλλικό οξύ ˙ ενώ ο όζος βελανιδιών περιέχει 45-50 % ταννικό οξύ. Και τα τρία επίσης περιέχουν υψηλές συγκεντρώσεις γαλλοταννικού οξέος. Στην εργασία μας, χρησιμοποιήσαμε όζους από βελανίδια και κούμαρα (τυπικοί όζοι δρυός) καθώς και όζους κυπαρισσιού (Εικόνα 1,2,3).
Και οι τρεις τύποι όζων μπορούν να βρεθούν σε όλη την Ευρώπη αλλά και οτιδήποτε περιέχει ταννίνες μπορεί να χρησιμοποιηθεί για την παραγωγή μελανιού ˙ π.χ. τσάι. Αλλιώς μπορείτε να χρησιμοποιήσετε ταννικό οξύ.
Θειικό οξύ ή καραμπογιά
Τα αρχαία χρόνια, η καραμπογιά (FeSO4.7H2O) εκχειλιζόταν με εξάτμιση του νερού από σιδηρούχα εδάφη. Αργότερα, στο τέλος του 16ου αιώνα, παραγόταν με προσθήκη θειικού οξέος σε ρινίσματα σιδήρου. Εμείς χρησιμοποιήσαμε θειικό σίδηρο μία κοινή ουσία σε ένα χημικό εργαστήριο.
Νερό
Καθώς το νερό βρύσης μπορεί να περιέχει προσμίξεις (όπως χλώριο) που αλλάζουν την ποιότητα του μελανιού, χρησιμοποιήσαμε αποσταγμένο νερό. Στην ιστορία, χρησιμοποιούταν κατά πάσα πιθανότητα νερό βροχής.
Αραβικό κόμμι
Το αραβικό κόμμι, ένα φυσικό κόμμι που εκχειλίζεται από την ακακία και χρησιμοποιείται σαν σταθεροποιητής τροφίμων, διατηρεί την ποιότητα του μελανιού με τρεις τρόπους :
- Διατηρεί το σύμπλοκο σιδήρου (την χρωστική ) αδιάλυτο
- Πυκνώνει το μελάνι και έτσι αποτρέπει την γρήγορη ροή του από το στυλό
- Ελαττώνει την ταχύτητα με την οποία το μελάνι εμποτίζει το χαρτί, δίνοντας καλύτερη και μακροβιότερη γραφή.
Υλικά και μέθοδοι
- Όζοι, 3 μέρη
- Νερό, 30 μέρη
- Θειικός σίδηρος, 2 μέρη
- Αραβικό κόμμι, 1 μέρος
|
|
|
|
Εικόνα 4: Κομματιασμένος όζος βελανιδιών |
Εικόνα 5: Φιτράρισμα του μίγματος νερού και θρυμματισμένων όζων |
|
|
|
|
Εικόνα 6. Τα τρία μελάνια |
Εικόνα 7. Τα αποτελέσματα! |
- Σπάστε τους όζους σε κομμάτια και μετά συνθλίψτε τους σε μύλο του καφέ (Εικόνα 4).
- Σε ένα ποτήρι ζέσεως, προσθέστε το νερό και τους κομματιασμένους όζους. Αφήστε το μίγμα να ζυμωθεί σε φωτεινό σημείο και θερμοκρασία δωματίου για 3 ημέρες.
- Φιλτράρετε το μίγμα (Εικόνα 5) και προσθέστε τον θειικό σίδηρο. Ανακατέψτε
καλά και αφήστε το για 3 ημέρες - Προσθέστε το αραβικό κόμμι, ανακατέψτε το μίγμα και έτοιμο το μελάνι σας.
Η εμπλεκόμενη χημεία
Αν και οι αντιδράσεις είναι εύκολες, η χημεία που εμπλέκεται είναι μάλλον πολύπλοκη. Αυτό το πείραμα δουλεύει καλύτερα αν οι νεότεροι μαθητές (14-15 ετών) κάνουν το εργαστηριακό κομμάτι, αφού οι μεγαλύτεροι μαθητές (17-18 ετών) τους εξηγήσουν τη χημεία και την βιολογία που εμπλέκεται.
Αφού οι όζοι κομματιάστηκαν, οι αντιδράσεις γίνονται σε δύο στάδια: η ζύμωση του γαλλοταννικού με το γαλλικό οξύ ακολουθούμενη από το σχηματισμό της χρωστικής του μελανιού.
Οι όζοι περιέχουν μεγάλα ποσά γαλλοτανικού οξέος (Εικόνα 8) αλλά χρειάζεται αναλογικά μικρή ποσότητα γαλλικού οξέος για το σχηματισμό της χρωστικής. Κατά το στάδιο της ζύμωσης, οι όζοι απελευθερώνουν το ένζυμο ταννάση από το Aspergillus niger και Penicillium glaucum, μύκητες που βρίσκονται μέσα στους όζους. Στις τρεις ημέρες, η ταννάση καταλύει την υδρόλυση του γαλλοτανικού οξέος σε γαλλικό οξύ και γλυκόζη (Εικόνα 9).
Μακροχρόνια φθορά
Το μελάνι από όζους σιδήρου μπορεί να χρησιμοποιείται εδώ και 1800 χρόνια, αλλά δεν μπόρεσε να περάσει το τεστ του χρόνου. Κατά τη διάρκεια των αιώνων, το μελάνι ξεθωριάζει, αποχρωματίζεται και καταστρέφει το χαρτί. Αυτό οφείλεται στην περίσσεια των ιόντων σιδήρου: η αναλογία 2:3 θειούχου σιδήρου προς όζους είναι λανθασμένη στοιχειομετρικά, με περισσότερο θειούχο σίδηρο να αντιδρά με το γαλλικό οξύ από όσο χρειάζεται.
Μερικά από αυτά τα πλεονάζοντα κατιόντα οξειδώνονται για να σχηματίσουν οξείδιο του σιδήρου (III), το οποίο καθώς είναι πιο αχνό από το σιδηρούχο πυρογαλλικό άλας, ξεθωριάζει το αρχικό μαύρο χρώμα της μελάνης. Άλλα κατιόντα σε περίσσεια καταλύουν μία καταστροφική αλυσιδωτή αντίδραση:
Fe2+ + O2 + H+ → Fe3+ + HOO–
Fe3+ + HOO– + H+ → Fe3+ + H2O2
Fe2+ + H2O2 → Fe3+ + HO– + OH– (Αντίδραση Fenton)
RH + HO– → R– + H2O
R– + O2 → ROO–
ROO– + R1H → ROOH + R1–
R1– + …..
όπου Fe2+ είναι πλεονάζον κατιόν σιδήρου, O2 είναι το ατμοσφαιρικό οξυγόνο και R είναι το ήμισυ της κυτταρίνης.
Επιπρόσθετα, όταν μία ρίζα HO– επιτίθεται την κυτταρίνη (RH) του χαρτιού, σπάει πολλούς δεσμούς και εμφανίζονται τρύπες. Στη συνέχεια, τα παραγόμενες ρίζες της κυτταρίνης (R–) αντιδρούν, σχηματίζοντας περισσότερες συνδέσεις, ώστε το κατεστραμμένο χαρτί να γίνεται πιο δικτυωτό, λιγότερο υδρόφιλο, και ως αποτέλεσμα πιο στεγνό και εύθραυστο.
Συντήρηση
|
|
Μία λύση στο πρόβλημα θεωρούταν η δημιουργία χηλικής ένωσης του σιδηρούχου κατιόντoς: η σύνδεση των σιδηρούχων κατιόντων με κατάλληλους συνδέσμους, μειώνει σημαντικά την οξείδωσή τους σε σιδηρικά κατιόντα, εμποδίζοντας την περαιτέρω καταστροφή. Όμως, η ανεύρεση του κατάλληλου χηλικού συνδέσμου ήταν μία πρόκληση: το EDTA, για παράδειγμα, δεν ελαττώνει το ρυθμό οξείδωσης του Fe2+. Πρόσφατη έρευνα στο Ινστιτούτο πολιτισμικής παράδοσης στην Ολλανδίαw2, όμως, δίνει ελπίδες. Μία επεξεργασία στηριζόμενη στο φυτικό οξύ (εξαορθοφωσφορικό άλας της μυοινοσιτόλης ˙ Εικόνα 12), ένα φυσικό αντιοξειδωτικό στους σπόρους, οδηγεί στο σχηματισμό ενός συμπλόκου Fe2+-φυτικού οξέος (Botti et al., 2005). Αυτό παρεμποδίζει την αντίδραση Fenton, ένα βήμα των αλυσιδωτών αντιδράσεων που περιγράφεται παραπάνω, και περιορίζει την περαιτέρω καταστροφή του χαρτιού. |
Συμπέρασμα
“Θα έρθει κάποια μέρα όπου ο χρόνος και η σχολαστική μελέτη πολλών γενεών θα αποκαλύψει αυτό που τώρα είναι κρυφό ˙ μία ζωή δεν θα είναι αρκετή για να τελειώσει μια τέτοια ατέρμονη έρευνα… και έτσι αυτά τα φαινόμενα θα αποσαφηνιστούν μετά από γενιές ερευνητών.. Θα έρθει κάποια μέρα που οι απόγονοί μας θα εκπλήσσονται που ήμασταν τόσο ανήξεροι για τόσο φανερά πράγματα. Πολλές ανακαλύψεις περιμένουν τις ερχόμενες γενιές όταν ακόμη και η μνήμη από εμάς θα έχει ξεθωριάσει. Ο κόσμος θα ήταν τιποτένιος, αν κάθε γενιά δεν έβρισκε κάποιο θέμα να διερευνήσει… Η φύση δεν αποκαλύπτει τα μυστικά της αβίαστα”
Seneca, Φυσικές ερωτήσεις, Βιβλίο VII
Αυτό το τοπικό απόσπασμα από τον Seneca (4 π.Χ – 65 μ.Χ) ισχύει ακόμη. Πιστεύω ότι ο Pliny θα ήταν ευχαριστημένος αν έβλεπε πως αυτή η γενιά είναι ικανή να αποκαλύψει αυτό που ο ίδιος δεν μπορούσε.
Αναφορές
Botti L, Mantovani O, Ruggiero D (2005) Calciumphytat zur Behandlung von Tintenfraß: Wirkungen auf das Papier (Ασβεστούχο φυτικό άλας, ένα φυσικό αντιοξειδωτικό για την αποτροπή της διάβρωσης του χαρτιού από το μελάνι σιδηρούχων όζων). Restaurator 26: 35-45
Αναφορές στο διαδίκτυο
w1 – ιστοσελίδα του National Geographic
w2 – ιστοσελίδα του Ινστιτούτου πολιτιστικής παράδοσης Ολλανδίας: www.icn.nl
Πηγές
Ιστοσελίδα οξείδωσης μελανιού : www.knaw.nl/ecpa/ink/index.html








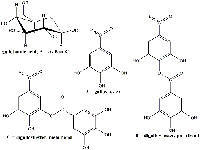 Εικόνα 8: Το γαλλοταννικό οξύ αποτελείται από ένα μόριο γλυκόζης, οι ομάδες υδροξυλίου του οποίου εστεροποιούνται από ένα μίγμα γαλλικού, διγαλλικού και πολυγαλλικού οξέος.
Εικόνα 8: Το γαλλοταννικό οξύ αποτελείται από ένα μόριο γλυκόζης, οι ομάδες υδροξυλίου του οποίου εστεροποιούνται από ένα μίγμα γαλλικού, διγαλλικού και πολυγαλλικού οξέος.
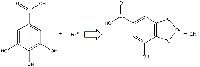 Εικόνα 10: Γαλλικό οξύ και κατιόντα σιδήρου αντιδρούν για να σχηματίσουν σιδηρούχο γαλλικό άλας.
Εικόνα 10: Γαλλικό οξύ και κατιόντα σιδήρου αντιδρούν για να σχηματίσουν σιδηρούχο γαλλικό άλας. Εικόνα 11: Το σιδηρούχο γαλλικό άλας αντιδρά με οξυγόνο για να δώσει σιδηρούχο πυρογαλλικό άλας και νερό
Εικόνα 11: Το σιδηρούχο γαλλικό άλας αντιδρά με οξυγόνο για να δώσει σιδηρούχο πυρογαλλικό άλας και νερό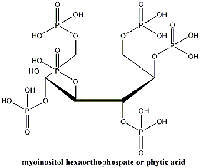
 Θαμμένο (300 μέτρα) Naica κάτω από το βουνό στο Chihuahuan Desert, αυτό το εκπληκτικό σπήλαιο ανακαλύφθηκε από δύο ανθρακωρύχους το 2000.
Θαμμένο (300 μέτρα) Naica κάτω από το βουνό στο Chihuahuan Desert, αυτό το εκπληκτικό σπήλαιο ανακαλύφθηκε από δύο ανθρακωρύχους το 2000.




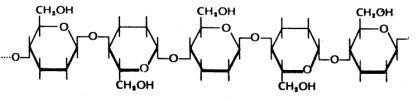


 ακτίνα).
ακτίνα). Από χημικής απόψεως είναι ανάλογο προς το τεχνητό μετάξι. Παρασκευάζεται με συμπίεση διαλυμάτων κυτταρίνης, συνήθως σε μορφή βισκόζης μέσα από λεπτή σχισμή σε κατάλληλο λουτρό αναγεννήσεως. Ετσι η κυτταρίνη λαμβάνεται με τη μορφή λεπτών διαφανών φύλλων. Αυτά μπορούν εύκολα να χρωματιστούν και χρησιμοποιούνται ως μέσα συσκευασίας.
Από χημικής απόψεως είναι ανάλογο προς το τεχνητό μετάξι. Παρασκευάζεται με συμπίεση διαλυμάτων κυτταρίνης, συνήθως σε μορφή βισκόζης μέσα από λεπτή σχισμή σε κατάλληλο λουτρό αναγεννήσεως. Ετσι η κυτταρίνη λαμβάνεται με τη μορφή λεπτών διαφανών φύλλων. Αυτά μπορούν εύκολα να χρωματιστούν και χρησιμοποιούνται ως μέσα συσκευασίας.




 Η χλωρίνη που είναι ισχυρό οξειδωτικό πρώτα οξειδώνει τις χρωμοφόρες ομάδες της βρωμιάς και τις κάνει αόρατες. Μετά από λίγο γίνεται η διάσπαση της βρωμιάς σε μικρά κομματάκια που διαλύονται στο νερό και απομακρύνονται τελικά από τα ρούχα.
Η χλωρίνη που είναι ισχυρό οξειδωτικό πρώτα οξειδώνει τις χρωμοφόρες ομάδες της βρωμιάς και τις κάνει αόρατες. Μετά από λίγο γίνεται η διάσπαση της βρωμιάς σε μικρά κομματάκια που διαλύονται στο νερό και απομακρύνονται τελικά από τα ρούχα. 



 Αυτά τα ένζυμα επιδρούν πάνω στους λεκέδες που είναι πρωτεϊνικής προέλευσης και τους αφαιρούν.
Αυτά τα ένζυμα επιδρούν πάνω στους λεκέδες που είναι πρωτεϊνικής προέλευσης και τους αφαιρούν.